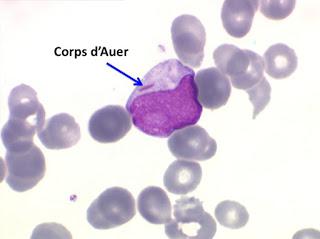
Le cytoplasme des blastes des leucémies aiguës myéloïde peut contenir une ou plusieurs inclusions spécifiques, les corps d'Auer. Le corps d'Auer a la forme d'un bâtonnet rougeatre, ressemblant à un bacille de Koch, constitué d'un paracristal de grains enzymatiques protéolytiques. (...).
Source iconographique et légendaire: http://cytologie-sanguine.com/image/LA_myeloides_gd/03-Corps-d'Auer(1).jpg
Nous avons recruté des patients diagnostiqués d’une leucémie aiguë myéloïde selon les critères de l’OMS et âgés de 18-70 ans inclus, dans notre établissement (Centre de Recherche sur le Cancer Fred Hutchison) pour inclusion dans cet essai de phase 1. Le critère principal de l’étude était l’innocuité de la perfusion de cellules progénitrices HLA-incompatibles en multiplication issues du sang ombilical après administration de clofarabine, cytarabine, et de facteur stimulant les colonies de granulocytes. Les inclusions sont maintenant terminées et une analyse per protocole a été effectuée. (…).
Entre le 29 juin 2010 et le 26 juin 2012, 29 patients atteints de leucémie aiguë myéloïde (19 sujets récemment diagnostiqués, dix sujets récidivants ou réfractaires) ont été recrutés. Les évènements indésirables les plus fréquemment relevés étaient fièvre (27 [93%] patients sur 29) et infections (25 [86%] patients sur 29). Nous avons observé un cas de toxicité aiguë infusionnelle (attribuée à une réaction allergique au diméthyle sulfoxide) parmi les 29 patients recrutés, qui ont reçu 42 perfusions de cellules progénitrices en multiplication. Les évènements indésirables additionnels graves - mais attendus – étaient les suivants (chacun d’entre eux chez un patient) : fibrillation auriculaire de grade 4, neutropénie fébrile de grade 4, infection pulmonaire accompagnée d’un nombre absolu de neutrophiles de grade 4, et un décès du fait d’une insuffisance hépatique. Aucune toxicité inattendue ou maladie du greffon versus l’hôte n’a été observée. Il n’y a eu aucune évidence de persistance de cellules progénitrices chez aucun patient au-delà de 14 jours, ou d’alloimmunisation induite.
La perfusion de cellules progénitrices en multiplication a semblé s’être effectuée en sécurité et pourrait représenter ainsi une méthode de traitement prometteuse chez les patients atteints de leucémie aiguë myéloïde. Dr Colleen Delanay, MD, et al, dans The Lancet Haematology, publication en ligne en avant-première, 7 juin 2016
Financement : Biomedical Advanced Research and Development Authority in the US Department of Health and Human Services et Genzyme (Sanofi).
Source: The Lancet Online / Traduction et adaptation: NZ
