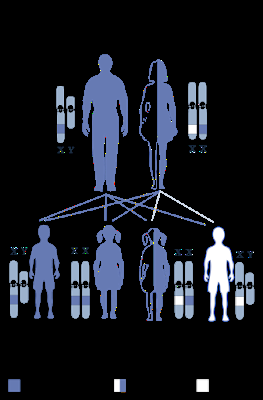
L'hémophilie A est une maladie due à une mutation du gène codant pour le facteur VIII de la coagulation, situé sur le chromosome X.
Carrier = porteur
Mother = Mère
Father = Père
Unaffected father = Père non atteint
Carrier Mother = Mère porteuse
Unaffected son = Fils non atteinte
Unaffected daughter = Fille non atteinte
Carrier daughter = Fille porteuse
Affected son = Fils atteint
Source: https://fr.wikipedia.org/wiki/H%C3%A9mophilie
L’emicizumab, un anticorps monoclonal humanisé, bispécifique, administré par voie sous-cutanée, est approuvé pour le traitement de personnes atteintes d’hémophilie A quel que soit leur âge et sans inhibiteurs du facteur VIII (FVIII). HAVEN 4 a évalué la prophylaxie par l’administration d’emicizumab à raison d’une dose toutes les 4 semaines chez les adultes et les adolescents atteints d’hémophilie A, abstraction faite du statut de l’inhibiteur FVIII.
Dans cette étude de phase 3 réalisée en 2 étapes, multicentrique, ouverte, des patients d’âge ≥ 12 ans, atteints de d’hémophilie A congénitale sévère (< 1% de l’activité FVIII normale dans le sang) ou d’hémophilie A avec inhibiteurs FVIII, placés sous traitement à base de concentrés de FVIII ou d’agents de dérivation, ont été recrutés dans trois sites situés au Japon et en Espagne pour constitution d’une cohorte de rodage, et dans 17 sites situés en Australie, Belgique, Japon, Pologne, Espagne et aux États-Unis pour constitution d’une cohorte d’expansion. Les participants des cohortes de rodage et d’expansion ont reçu de l’emicizumab par voie sous-cutanée à raison de 6 mg / kg toutes les 4 semaines sur une période de 24 semaines ou plus ; pour les patients intégrés dans la cohorte d’expansion, ce régime était précédé de quatre doses de charge de 3 mg / kg par semaine. Dans la cohorte de rodage, nous avons évalué la pharmacocinétique après injection unique et injections multiples (toutes les 4 semaines) par voie sous-cutanée de 6 mg / kg d’emicizumab, ainsi que l’innocuité. Dans la cohorte d’expansion, le critère d’efficacité était l’efficacité de l’administration par voie sous-cutanée de l’emicizumab en prophylaxie pour le maintien d’une prévention adéquate des hémorragies, exprimée en taux annualisé d'hémorragies après traitement, d'hémorragies (traitées et non traitées), d'hémorragies spontanées traités, d'hémorragies articulaires traitées, et d'hémorragies articulaires cibles traitées ; chez tous les patients qui avaient reçu au moins une dose d’emicizumab. L’innocuité était évaluée chez tous les participants qui avaient reçu de l’emicizumab. (…).
Entre le 30 janvier 2017 et le 27 février 2017, sept patients ont été intégrés dans la cohorte initiale de rodage, qui a confirmé le profil pharmacocinétique et d’innocuité du régime de traitement basé sur des simulations modélisées, fournissant des évidences suffisantes pour l’ouverture d’une cohorte d’expansion (n=41), dont le recrutement et l’intégration ont eu lieu entre le 24 mai 2017 et le 30 juin 2017. Le taux annualisé de hémorragies traités était de 204 (Intervalle de Confiance [IC] 95% 1.4-4.3). 23 (56.1% ; IC 95% 39.7-71.5) patients sur 41 n’ont rapporté aucun traitement pour saignement et 37 (90% ; 76.9-97.3) ont rendu compte de zéro à trois hémorragies traitées. Le taux annualisé d'hémorragies était de 4.5 (IC 95% 3.1-6.6) pour tous hémorragies, 0.6 (0.3-1.5) pour les hémorragies spontanées, 1.7 (0.8-3.7) pour les hémorragies articulaires, et 1.0 (0.3-3.3) pour les hémorragies articulaires cibles. Les événements indésirables liés au traitement les plus fréquemment relevés étaient des réactions au niveau du site d’injection (neuf [22%] patients sur 41). Nous n’avons observé aucun événement thrombotique ou de développement de novo d’anticorps anti-médicament du fait du potentiel neutralisant des inhibiteurs FVIII.
L’emicizumab administré une fois toutes les 4 semaines a permis un contrôle significatif des hémorragies tout en étant bien toléré. Ce traitement pourrait apporter une amélioration des soins prodigués aux patients en allégeant les traitements et en augmentant l’adhésion à une prophylaxie efficace ; potentiellement en diminuant le développement de complications secondaires chez les personnes atteintes d’hémophilie A. Prof Steven W Pipe, MD, et al, dans The Lancet Haematology, publication en ligne en avant-première, 16 avril 2019
Financement: F Hoffmann-La Roche et Chugai PharmaceuticalSource : The Lancet Online / Traduction et adaptation : NZ
