Le médicament expérimental Enhoxy® de la biotech française Erytech Pharma vient de recevoir, du Comité des médicaments orphelins (COMP) de l'Agence européenne du médicament (EMA), le statut de médicament orphelin pour le traitement de la drépanocytose. Ce statut devrait lui permettre « de passer » dès l'année prochaine en phase d'essai clinique et de représenter très rapidement, pour les 80.000 patients européens atteints, une nouvelle alternative thérapeutique aux échanges de sang nécessaires aux patients drépanocytaires.
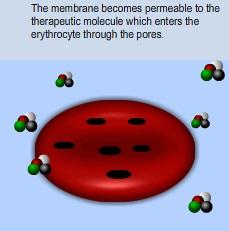
Enhoxy®, des érythrocytes ou globules rouges humains qui encapsulent (cliquer sur visuel ci-contre) un ingrédient actif, l'inositol héxaphosphate, permet d'améliorer l'oxygénation des globules rouges. Le manque d'oxygène dans le sang est associé à la malformation des cellules sanguines et à des crises d'hypoxie. Des échanges érythrocytaires ou échanges de sang total sont parfois nécessaires pour inverser ces crises et les conditions hypoxiques chez les patients drépanocytaires. Enhoxy® permet de réduire le nombre de transfusions sanguines nécessaires.
Des essais cliniques dès l'année prochaine : Cette désignation de statut de médicament orphelin (Orphan Drug Designation- ODD) garantit 10 ans d'exclusivité commerciale après autorisation de mise sur le marché (AMM) dans tous les Etats membres de l'UE, un processus d'évaluation réglementaire simplifié et des réductions de taxes. Avec déjà de nombreuses données d'études expérimentales, Erytech, spécialisé dans le développement de traitements en oncologie et pour les maladies rares, compte engager les essais cliniques dès l'année prochain dont le médicament phare, Graspa® pour le traitement de la leucémie aiguë lymphoblastique a déjà reçu la désignation de médicament orphelin en Europe et aux Etats-Unis et est en cours d'essai clinique de phase II / III en Europe.
Sources: EMA, Communiqué Erytech

