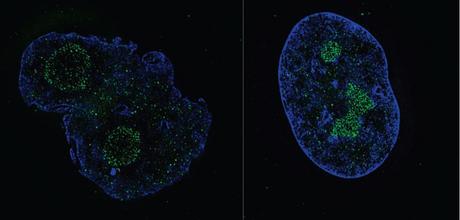
À gauche, cette cellule d’un patient atteint de la Progeria est déformée. À droite, cette cellule traitée avec la remodeline présente une architecture normale.
Des chercheurs viennent d’identifier une molécule prometteuse contre le syndrome de Hutchinson-Gilford ou Progeria, une maladie génétique rare qui provoque le vieillissement prématuré chez l’enfant et son décès avant l’âge adulte.
Bébés amaigris aux cheveux clairsemés et aux veines apparentes, enfants aux allures de vieillards… Les symptômes associés au syndrome de Hutchinson-Gilford, une maladie génétique non héréditaire provoquant un vieillissement accéléré, ne peuvent laisser indifférents. La Progeria, le nom couramment donné à cette maladie spectaculaire qui touche environ 300 enfants dans le monde, a inspiré des films de cinéma comme L’Étrange Histoire de Benjamin Button. Mais, si le personnage interprété par l’acteur Brad Pitt rajeunit d’années en années et mène une vie longue et bien remplie, aujourd’hui, l’espérance de vie des enfants atteints de ce syndrome ne dépasse pas 13 ans en moyenne.
Un véritable condensé des maux de la vieillesse
Pendant plus d’un siècle, les médecins ont assisté, impuissants, aux ravages de cette maladie décrite pour la première fois en 1887. « Le premier symptôme est une inversion de la courbe de poids et se manifeste entre 6 et 12 mois », décrit Delphine Larrieu, chercheuse au Gurdon Institute de Cambridge et spécialiste de la Progeria. Lorsqu’ils grandissent, la taille des malades ne dépasse pas 1,10 m pour un poids de 15 kilos. Viennent s’ajouter à ces désordres le cholestérol, des fragilisations osseuses comme l’arthrose et l’ostéoporose, et les maladies cardio-vasculaires qui finissent par provoquer la mort, puisque les malades décèdent généralement d’une crise cardiaque. Un véritable condensé des maux de la vieillesse, à une exception près : le développement cognitif des enfants atteints reste, lui, parfaitement normal.
Depuis le début des années 2000, les progrès de la biologie moléculaire ont relancé les recherches sur la maladie et la possibilité d’un traitement. En 2003, la mutation responsable de la maladie a été identifiée par une équipe de l’Inserm sur le gène Lamina. « Ce gène code habituellement pour une protéine, la lamine. Du fait de la mutation, une forme anormale de la lamine, appelée progérine, est exprimée : c’est l’accumulation de cette protéine qui est toxique et provoque la maladie », explique Sébastien Britton, chercheur à l’Institut de pharmacologie et de biologie structurale[1]. Au niveau cellulaire, les désordres causés par la progérine sont tout aussi spectaculaires que les symptômes visibles chez l’enfant : au lieu d’être bien rond, le noyau logé à l’intérieur de la cellule est déformé, et l’ADN qu’il contient est désorganisé.
Une molécule thérapeutique identifiée
Le gène défaillant ayant été identifié, la première voie thérapeutique suivie par les chercheurs a consisté à bloquer les effets de la mutation en empêchant la formation de la lamine anormale. « Pour devenir mâture, la lamine normale se lie à une chaîne d’acides gras appelée groupement farnésyl, qui se détache ensuite de la protéine, explique Sébastien Britton. Dans le cas de la progérine, le groupement farnésyl reste attaché à la protéine. » L’objectif est donc d’empêcher que cette association se fasse. Pour ce faire, des chercheurs ont identifié une molécule appelée inhibiteur de farnésyl transférase, déjà utilisée dans certains traitements pour le cancer. Des essais cliniques sont en cours et ont redonné espoir aux parents d’enfants malades. Les premiers résultats montrent une reprise de poids et/ou une petite amélioration au niveau des os et des vaisseaux sanguins, avec un gain d’espérance de vie d’environ un an.
C’est une approche radicalement différente qui fait parler d’elle ces jours-ci. Un groupe de chercheurs, conduits par Delphine Larrieu, a en effet décidé de prendre le problème à l’envers : au lieu de s’intéresser aux mécanismes de la maladie, afin d’en déduire un traitement, ils ont voulu s’attaquer à ses conséquences visibles sur la cellule (phénotype), et notamment à la déformation du noyau. « Nous avons testé une quinzaine de molécules connues pour avoir un effet sur l’organisation de l’ADN, explique la chercheuse, qui a cosigné avec Sébastien Britton un article paru dans Science en mai 2014[2]. Parmi elles, une candidate sérieuse, la remodeline, a démontré son efficacité : elle recompacte la chromatine, l’emballage de l’ADN, et rétablit la forme circulaire du noyau. » Conséquence : les performances de la cellule, notamment la durée de vie et la capacité à se diviser, sont améliorées.
Reste maintenant à développer la molécule thérapeutique et à conduire des essais cliniques. La route est encore longue, mais les chercheurs pourront vraisemblablement compter sur l’appui de laboratoires pharmaceutiques, pourtant réputés frileux lorsqu’il s’agit de maladies orphelines. C’est que les cellules affectées par le syndrome de Hutchinson-Gilford partagent avec les cellules vieillissantes « normales » un certain nombre de points communs : noyau déformé, ADN décompacté, division cellulaire ralentie, etc. En réussissant à soigner les malades atteints de la Progeria, l’espoir de gommer également certains des symptômes du vieillissement naturel, comme les problèmes osseux, la perte de cheveux ou la moindre résistance du cœur, est réel…
(01-07-2014 - par Laure Cailloce, Cnrs)
Notes
1. Unité CNRS/UPS.
2. « Chemical Inhibition of NAT10 Corrects Defects of Laminopathic Cells », D. Larrieu, S. Britton, M. Demir, R. Rodriguez et S. P. Jackson., Science, 2 mai 2014, vol. 344 (6183) : 527-532.

