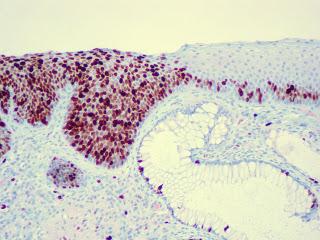
Carcinome de l'anus in situ.
Source iconographique: https://de.wikipedia.org/wiki/Carcinoma_in_situ#/media/File:Anal_squamous_carcinoma_in_situ,_Ki-67_immunostain.jpg
Nous avons effectué cette étude de phase 2 multicentrique à simple bras dans dix centres hospitalo-universitaires situés aux États-Unis d’Amérique. Nous avons recruté des patients atteints de CCSCA métastatique réfractaires aux traitements, à qui on a administré du nivolumab à raison de 3 mg/kg toutes les 2 semaines. Le critère principal d’évaluation était la réponse au traitement selon les critères RECIST version 1.1, dans la population en intention de traiter. Au moment de la collecte des données, l’étude était toujours en cours, et les patients continuaient à recevoir le traitement. (…).
Nous avons dépisté 39 patients, dont 37 ont été recrutés et ont reçu au moins une dose de nivolumab. Parmi les 37 patients, neuf(24% Intervalle de Confiance [IC] 95% 15-33) ont présenté des réponses. Deux réponses complètes et sept réponses partielles ont été dénombrées. Les événements indésirables de grade 3 rapportés étaient anémie (n=2), fatigue (n=1), éruption cutanée (n=1), et hypothyroïdisme (n=1). Aucun événement indésirable grave n’a été relevé.
Il s’agit ici du premier essai de phase2 d’immunothérapie du CCSCA, totalement bouclé à notre connaissance. Le blocage des points de contrôle immunitaires semble représenter une approche prometteuse pour le traitement de patients atteints de cette maladie orpheline. Van K Morris, MD, et al, dans The Lancet Oncology, publication en ligne en avant-première, 17 février 2017
Financement : Institut National du Cancer / Programme d’Évaluation Thérapeutique du Cancer, Fondation de recherche sur le Cancer Anal et le Cancer HPV, Fonds E.B. pour le Cancer Anal, Programme MD Anderson Moon Shots de l’Université du Texas, donneur philantropique anonyme.
Source : The Lancet Online / Traduction et adaptation : NZ
