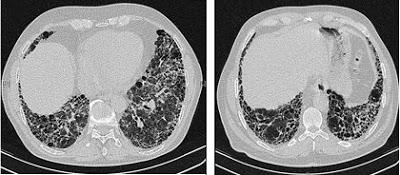
Tomodensitométrie thoracique d'un patient atteint de Fibrose Pulmonaire Idiopathique
Source : https://commons.wikimedia.org/wiki/File:HR_tomography_of_the_chest_of_an_IPF_patient.jpg
Le risque de fibrose pulmonaire idiopathique (FPI) possède une forte composante génétique. Des études montrent l’implication de variations au niveau de plusieurs loci, incluant TERT, des gènes possédant des propriétés surfactantes, et un polymporphisme à nucléotide simple au niveau CHR11P15 (rs35705950) dans la région intergénique entre TOLLIP et MUC5B. Des patients atteints de FPI qui présentent des allèles de prédisposition à des maladies au niveau de rs35705950 présentent une meilleure survie à partir du moment du diagnostic de PFI que les patients homozygotes pour les allèles « non à risque », alors que les patients porteurs de télomères plus courts présentent des durées de survie plus courtes. Notre but était d’évaluer si les variants modificateurs de protéines chez les gènes de régulation de la longueur des télomères sont présents en plus grand nombre chez les patients atteints de FPI homozygote pour les allèles « non à risque » au niveau de rs35705950.
Entre le 1er novembre 2014 et le 1ernovembre 2016, nous avons examiné des échantillons de sang prélevés chez des patients d’ascendance européenne âgés de 40 ans ou plus atteints de FPI inclus dans trois essais cliniquesinternationaux de phase 3 (INSPIRE, CAPACITY, ASCEND), dans un étude de phase 2 (RIFF), et dans des essais observationnels réalisés aux États-Unis (Registre des sujets atteints de Maladies Pulmonaires Interstitielle de la Clinique Vanderbilt, le Registre des Cohortes de sujets atteints de Maladies Pulmonaire Interstitielles de l’UCSF) à l’Institut Broad (Cambridge, MA, USA) et Human Longevity (San Diego, CA, USA). Nous avons également examiné des échantillons de sang prélevés chez des sujets non atteints de FPI dans plusieurs essais cliniques. Nous avons effectué des séquençages de génome entier afin d’évaluer la longueur des télomères et identifiant les variants de gènes modificateurs de protéines rares, stratifiés par génotype rs35705950. Nous avons aussi examiné des variations fonctionnelles rares chez les exons TERT et comparé la longueur des télomères et la progression de la maladie à travers les génotypes.
Nous avons examiné les échantillons de 1510 patients atteints de FPI et de 1870 contrôles non atteints de FPI. 30 (3%) patients sur 1 046 avec risque de maladie lié à un allèle, présentaient un variant fonctionnel rare dans TERT en comparaison des 34 (7%) patients sur 464 porteurs d’allèles non à risque (odds ratio [OR] 0.40 [Intervalle de Confiance -IC- 95% 0.24-0.66], p=0.00039). Des analyses supplémentaires ont identifié une quantité plus importante de variants rares de gènes modificateurs de protéines chez les gènes PARN et RTEL1, et de rares variations chez TERC chez les patients atteints de FPI en comparaison des contrôles. Nous avons amplifié notre étude de population pour fournir une meilleure estimation de la fréquence des variants rares dans ces quatre loci, et pour calculer la longueur des télomères. La proportion de patients avec au moins un variant rare de gène TERT, PARN, TERC, ou RTEL1 était plus élevée chez les patients atteints de FPI que chez les contrôles (149 (9%) sur 1 739 patients versus 205 [2%] sur 8 645 contrôles, p=2.44 x 10-8). Les patients atteints de FPI et qui présentaient un variant, quel qu’en soit le gène concerné parmi les quatre gènes de télomérase identifiés, développaient des télomères qui étaient de 3.69 à 16.10 % plus courts que les patients sans variant dans aucun des quatre gènes ; et, de plus, présentaient un âge moyen de début de maladie plus précoce (65.1 ans [Déviation Standard -DS- 7.8] versus67.1 ans [7.9], p=0.004). Au niveau des bras placebo des essais cliniques, des télomères plus courts étaient associés à une progression plus rapide de la maladie (+1.7% de capacité vitale forcée par kb par an, p=0.002). Le pirfenidone a apporté des bénéfices, abstraction faite de la longueur des télomères. (p=4.24 x 10-8 pour une longueur de télomère inférieure à la médiane, p=0.0044 pour une longueur de télomère supérieure à la médiane).
Des variants de gènes modificateurs de protéines rares des gènes TERT, PARN, TERC, and RTEL1 sont présents en plus grand nombre chez les patients atteints de FPI par rapport aux contrôles, et, dans le cas de TERT, plus particulièrement chez les sujets sans allèle à risque au niveau du locus rs35705950. Cela suggère que de multiples facteurs génétiques contribuent au déclenchement de la FPI sporadique, pouvant impliquer des mécanismes de pathogénèse et de progression de la maladie distincts. Amy Dressen, MS, et al, dans The Lancet Respiratory Medicine, Early Online Publication, 8 juin 2018
Financement : Genentech, National Institutes of Health, Francis Family Foundation, Pulmonary Fibrosis Foundation, Nina Ireland Program for Lung Health, US Department of Veterans Affairs.
Source : The Lancet Online / Traduction et adaptation : NZ
