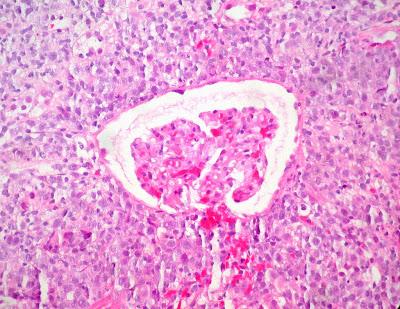
Long historique de leucémie lymphoïde chronique avec syndrome de Richter patent, révélant une masse de 8 cm de diamètre sur le rein par tomodensitométrie; masse inexistante une année auparavant.
Source iconographique: https://www.flickr.com/photos/euthman/19337925450
Des études précliniques ont montré des effets antitumoraux synergiques entre l’ibrutinib et l’inhibition du point de contrôle immunitaire. Le but de cette étude était d’évaluer l'innocuité et l’activité de l’ibrutinib en combinaison avec le nivolumab chez des patients atteints de maladies malignes des cellules B récidivantes ou réfractaires.
Nous avons effectué une étude de phase 1/2a en deux parties, en ouvert, dans 21 hôpitaux situés en Australie, Israël, Pologne, Espagne, Turquie, et aux États-Unis. L’objectif principal de la partie A de l’essai (à dose croissante) était d’évaluer l’innocuité de l’administration quotidienne per os d’ibrutinib (420 mg ou 560 mg) en combinaison avec le nivolumab par voie intraveineuse (3 mg/kg toutes les 2 semaines) pour définir une dose à recommander pour la réalisation d’un essai clinique de phase 2 chez des patients atteints de leucémie lymphoïde chronique récidivante ou réfractaire à haut risque ou de lymphome à petits lymphocytes (del17p ou del11q), de lymphome folliculaire, ou lymphome diffus à grandes cellules B. L’optimisation de la dose à administrer était investiguée à l’aide d’un modèle modifié de probabilité de toxicité. L’objectif principal de la partie B de l’essai, dite phase d’expansion, était d’établir l’activité préliminaire (c’est-à-dire la proportion de patients obtenant une réponse globale au traitement) suite à l’administration du cocktail ibrutinib + nivolumab sur 4 cohortes de patients : patients atteints de leucémie lymphoïde chronique à haut risque ou lymphome lymphocytaire à petits lymphocytes (del17p ou del11q), lymphome folliculaire, ou lymphome diffus à grandes cellules B, et transformation en Syndrome de Richter. Tous les participants qui avaient reçu au moins une dose de traitement étaient inclus dans l’analyse principale et les analyses étaient réalisées par cohorte de patients, établies selon la pathologie dont ils étaient atteints. (…).
Entre le 12 mars 2015 et le 11 avril 2017, 144 patients ont été recrutés dans l’étude. Trois patients sont décédés avant de recevoir le traitement à l’étude ; ainsi, 141 patients ont été inclus dans l’analyse, 14 dans la partie A, et 127 dans la partie B. Une toxicité dose-limitante (hyperbilirubinémie de grade 3) a été rapportée sous administration de la dose de 420 mg dans la cohorte composée de patients atteints de lymphome diffus à grandes cellules B, résolue 5 jours plus tard. La combinaison (cocktail) ibrutinib + nivolumab a conduit à des réponses globales chez 22 (61%) patients sur les 36 atteints de leucémie lymphoïde chronique à haut risque ou lymphome lymphocytaire à petits lymphocytes, chez 13 (33%) patients sur les 40 atteints de lymphome folliculaire, chez 16 (36%) patients sur les 45 atteints de lymphome diffus à grandes cellules B, et chez 13 (65%) patients sur les 20 patients ayant évolué en Richter. Les évènements indésirables tous grades confondus les plus communément rencontrés étaient diarrhée (47 [33%] sur 141 patients), neutropénie (44 [31%]), et fatigue (37 [26%]). 11 (8%) patients sur 141 ont présenté des événements indésirables conduisant au décès ; aucun d’entre eux n’était imputable au médicament à l’étude. Les événements indésirables de grade 3-4 les plus communément rencontrés étaient neutropénie (40 [28%] patients sur 141) et anémie (32 [23%]). La fourchette d’incidence des neutropénies de grade 3-4 allait de huit (18%) patients sur les 45 atteints de lymphome diffus à grandes cellules B à 19 (56%) patients sur les 36 atteints de leucémie lymphoïde chronique ; la fourchette d’incidence des anémies de grade 3-4 allait de cinq (13%) patients sur 40 patients atteints de lymphome folliculaire à sept (35%) patients sur 20 patients atteints d’une pathologie évoluant vers un syndrome de Richter. Les événements indésirables graves les plus communément relevés comprenaient anémie (six [4%] patients sur 141) et pneumonie (cinq [4%]). Les événements indésirables de grade 3-4 liés à des réactions immunitaires étaient éruption cutanée (six [4%] patients sur 141) et augmentation de l’alanine aminotransférase (trois [2%]).
La combinaison d’ibrutinib et de nivolumab a présenté un profil d’innocuité et d’activité préliminaire rapportées similaires à celles obtenues avec ibrutinib uniquement dans les cas de leucémie lymphoïde chronique ou de lymphome lymphocytaire à petites cellules, et de lymphome diffus à grandes cellules B. La réponse clinique chez les patients dont la pathologie avait évolué en syndrome de Richter s’est révélée prometteuse et justifie de futures évaluations cliniques. Anas Younes, MD, et al, dans The Lancet Haematology, publication en ligne en avant-première, 11 janvier 2019
Financement : Janssen R&D
Source : The Lancet Online / Traduction et adaptation : NZ
