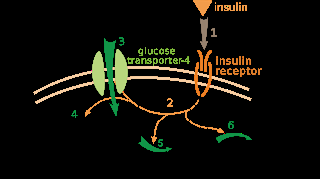
L'insuline se lie à son récepteur, induisant une cascade d'activation de protéines, conduisant notamment à la translocation du transporteur de glucose insulino-sensible, permettant ainsi la captation du glucose vers l'intérieur de la cellule, son stockage en glycogène ou sa transformation en pyruvate et en acide gras.
Source: https://commons.wikimedia.org/wiki/File:Insulin_glucose_metabolism_ZP.svg
L’insuline administrable per os 338 (I338) est un analogue de l’insuline à action prolongée (de base) formulé en comprimé comprenant également caprate de sodium comme activateur d’absorption. Nous avons poursuivi des investigations relatives à l’efficacité et l’innocuité de I338 versus insuline glargine (IGlar) administrée par voie sous-cutanée chez des patients atteints de diabète de type 2.
Il s’agissait d’une étude de phase 2 à groupes parallèles, effectuée en double-aveugle, double-placebo et contrôlée par médicament actif sur une période de 8 semaines, dans deux instituts de recherche situés en Allemagne. Des patients atteints de diabète de type 2, n’ayant jamais reçu d’insuline, non-adéquatement contrôlés par de la metformine en monothérapie, ou combinés avec d’autres médicaments antidiabétique administrés per os (HbA1c7.0-10.0% ; IMC 25.0-40.0 kg/m2), ont été répartis de manière aléatoire (1:1) pour recevoir une dose quotidienne de I338 + placebo par voie sous-cutanée (groupe I338) ou IGlar une fois par jour plus le placebo (groupe IGlar). La randomisation était réalisée à l’aide d’un système interactif de réponse par internet stratifié en fonction du traitement antidiabétique administré per os à la ligne de base. Ni les patients ni les investigateurs n’avaient accès au tableau de randomisation. La titration de la dose d’insuline à administrer visait à atteindre une concentration plasmatique de glucose à jeun se situant entre 4.4-7.0 mmol/L. Les doses initiales recommandées étaient de 2700 nmol de I338 ou 10 U IGlar, et les doses maximales admises pour administration au cours de l’essai étaient de 16 200 nmol de I338 ou 60 U IGlar. Le critère principal était la différence de concentration plasmatique de glucose à jeun à 8 semaines entre les groupes de traitements, avec prise en compte de tous les patients qui avaient reçu au moins une dose du médicament à l’étude (c’est-à-dire sur l’ensemble d’analyse intégral). Cet essai est maintenant terminé (…).
Entre le 1er juin et le 19 octobre 2015, 82 patients ont été examinés en vue de leur admissibilité pour participer à l’étude ; et 50 ont été retenus et répartis de manière aléatoire pour rejoindre le groupe I338 (n=25) ou le groupe IGlar (n=25). La moyenne de concentration plasmatique de glucose à jeun était de 9.7 (Déviation Standard -DS- 2.8) dans le groupe I338 et de 9.1 (1.7) dans le groupe IGlar. Les moyennes de concentrations plasmatiques de glucose à 8 semaines, calculées par la méthode des moindres carrés, étaient de 7.1 mmol/L (Intervalle de Confiance [IC] 95% 6.4-7.8) dans le groupe I338 et de 6.8 mmol/L (6.5-7.1) dans le groupe IGlar, sans différence significative entre les traitements (0.3 mmol/L [de -0.5 à 1.1] ; p=0.46). I338 et IGlar ont été bien tolérés par les patients, d’une manière générale. Des évènements indésirables ont été rapportés par 15 (60%) patients du groupe I338 et par 17 (68%) patients du groupe IGlar. Les évènements indésirables les plus communément rencontrés étaient diarrhée (trois [12%] patients dans chaque groupe) et nasopharyngite (cinq [20%] dans le groupe I338 et deux [8%] dans le groupe IGlar). La plupart des évènements indésirables ont été évalués comme bénins (47 évènements sur 68), et aucun évènement indésirable grave n’a été rapporté. (…). L’incidence d’hypoglycémie était faible dans les deux groupes (n=7 évènements dans le groupe I338 ; n=11 dans le groupe IGlar), sans épisodes sévères.
I338 apporte une amélioration dans le contrôle de la glycémie en toute sécurité, chez des patients atteints de diabète de type 2 naïfs de tout traitement insulinique ; sans évidence d’une différence d’efficacité en comparaison de l’insuline glargine, type d'insuline basale fréquemment administrée par voie sous-cutanée. La poursuite du développement de cette insuline en particulier, administrable per os, a été annulé du fait que les doses de I338 à administrer étaient élevées et, donc, la production des quantités requises pour prescription à un large public a été jugé non viable sur le plan commercial. L’amélioration des technologies impliquées dans le développement du produit est l’objectif de la recherche actuelle. Inge B Halberg, PhD, et al, dans The Lancet Diabetes & Endocrinology, publication en ligne en avant-première, 21 janvier 2019
Financement : Novo Nordisk
Source : The Lancet Online/ Traduction et adaptation : NZ
