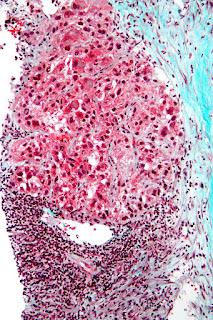
Carcinome hépatocellulaire [bien différencié, haut du cliché; peu différencié, bas du cliché]
Source iconographique: https://en.wikipedia.org/wiki/Hepatocellular_carcinoma
Le nivolumab en monothérapie a montré des réponses durables, une sécurité gérable et une survie prometteuse chez les patients atteints d'un carcinome hépatocellulaire avancé dans l'étude de phase 1–2 CheckMate 040. Notre objectif était d'étudier le nivolumab en monothérapie par rapport au sorafénib en monothérapie en première intention chez les patients atteints d'un carcinome hépatocellulaire avancé.
Dans cet essai de phase 3 randomisé, en ouvert, réalisé dans des centres médicaux de 22 pays et territoires en Asie, en Australasie, en Europe et en Amérique du Nord, des patients âgés d'au moins 18 ans atteints d'un carcinome hépatocellulaire avancé confirmé histologiquement [non éligibles pour, ou dont la maladie avait progressé après une intervention chirurgicale ou un traitement locorégional ; sans traitement systémique antérieur pour le carcinome hépatocellulaire, avec un score de performance de classe A de Child-Pugh et du groupe d'oncologie coopérative de l'Est de 0 ou 1, et quel que soit le statut d'hépatite virale] ont été assignés au hasard (1:1) via un système de réponse vocale interactif pour recevoir nivolumab (240 mg par voie intraveineuse toutes les 2 semaines) ou sorafénib (400 mg par voie orale deux fois par jour) jusqu'à progression de la maladie ou toxicité inacceptable. Le critère d'évaluation principal était la survie globale évaluée dans la population en intention de traiter. L'innocuité a été évaluée chez tous les patients ayant reçu au moins une dose du médicament à l'étude.
Entre le 11 janvier 2016 et le 24 mai 2017, 743 patients ont été randomisés pour recevoir un traitement (nivolumab, n=371 ; sorafenib, n=372). Lors de l'analyse principale, le suivi médian de la survie globale était de 15,2 mois (Intervalle Interquartile [IQR] 5,7–28,0) pour le groupe nivolumab et de 13,4 mois (5,7–25,9) dans le groupe sorafénib . La survie globale médiane était de 16,4 mois (Intervalle de Confiance [IC] 95 % 13,9–18,4) avec le nivolumab et de 14,7 mois (11,9–17,2) avec le sorafenib (hazard ratio 0,85 [IC 95 % 0,72–1,02] ; p=0,075 ; suivi minimal de 22,8 mois) ; le niveau de signification défini par le protocole de p = 0,0419 n'a pas été atteint. Les événements indésirables de grade 3 ou plus liés au traitement les plus fréquents ont été l'érythrodysesthésie palmo-plantaire (1 [< 1 %] des 367 patients du groupe nivolumab versus52 [14 %] des patients du groupe sorafénib), l'augmentation de l'aspartate aminotransférase (22 [6%] versus 13 [4%]), et l'hypertension (0 versus26 [7%]). Des événements indésirables graves liés au traitement ont été rapportés chez 43 (12 %) patients recevant du nivolumab et 39 (11 %) patients recevant du sorafénib. Quatre décès dans le groupe nivolumab et un décès dans le groupe sorafénib ont été évalués comme étant liés au traitement.
Le traitement de première intention par le nivolumab n'a pas significativement amélioré la survie globale par rapport au sorafénib, mais une activité clinique et un profil de sécurité favorable ont été observés chez les patients atteints d'un carcinome hépatocellulaire avancé. Ainsi, le nivolumab pourrait être considéré comme une option thérapeutique pour les patients chez qui les inhibiteurs de la tyrosine kinase et les médicaments antiangiogéniques sont contre-indiqués ou présentent des risques importants. Thomas Yau, MD, et al, dans The Lancet Oncology, publication en ligne en avant-première, 13 décembre 2021
Financement : Bristol Myers Squibb en collaboration avec Ono Pharmaceutical
Source : The Lancet Online / Préparation post : NZ
